Tutti gli essere umani presentano anomalie nel proprio DNA. Nella maggior parte dei casi queste non hanno alcuna conseguenza. Alcune, però, sono responsabili di patologie, sindromi gravi, predisposizione a malattie. È sulla ricerca di questi difetti e del loro significato che si concentra la genetica medica i cui progressi sono costanti grazie all’evoluzione tecnologica: « La possibilità di queste indagini – spiega il dottor Rosario Casalone, primario dell’unità operativa dipartimentale SMEL specializzato in Citogenetica e Genetica Medica, dell‘Ospedale di Circolo di Varese afferente al Dipartimento Materno Infantile – è strettamente legata alle innovazioni tecnologiche. È un ambito di studio in continua evoluzione e negli ultimi due anni sono state introdotte metodologie di indagine che hanno permesso enormi passi avanti».
Sono due le novità tecnologiche che stanno fornendo i maggiori risultati di utilità clinica: la tecnologia array-CGH e quella chiamata “Next Generation Sequencing” (NGS). La prima è già proficuamente utilizzata, anche dall’Ospedale di Varese, sia in epoca postnatale per la identificazione delle cause di ritardo mentale e malformazioni congenite, sia in epoca prenatale in casi selezionati, mentre la seconda inizia soltanto ora a trovare una applicazione clinica: « Queste indagini sono complesse e hanno sempre bisogno di essere interpretate da un genetista esperto. Il nostro è inoltre davvero un lavoro trasversale di equipe che coinvolge anche specialisti di altre discipline, a seconda del campo di indagine. Questi costosi test devono essere effettuati soltanto dopo un inquadramento clinico dei pazienti e delle varie situazioni tramite una visita di genetica medica».
I test genetici vengono sempre preceduti e seguiti da un colloquio con lo specialista in genetica: « È importante illustrare ai pazienti il tipo di esame che si effettua, ciò che esso permette di identificare ed i suoi limiti diagnostici, così da arrivare a un consenso informato. I risultati ottenuti invece, devono essere estesamente spiegati ai pazienti perchè i referti delle due innovative indagini array-CGH e NGS, sono molto complessi.».
« Le malattie genetiche sono ereditarie – spiega il dottor Casalone – per cui il paziente deve essere disponibile a coinvolgere anche il resto della famiglia. Le regole per la privacy quindi sono molto stringenti. Nel consenso informato sottoscritto dai pazienti, si affronta anche il problema della conservazione del DNA per eventuali supplementi di indagine».
 Attualmente, le indagini genetiche non sono in grado di evidenziare la causa di tutte le malformazioni congenite o del ritardo mentale. « Il 50% delle patologie genetiche non ha ancora una causa definita. I tests citati precedentemente aumentano del 20% o più, la possibilità di diagnosticarne la causa. L’ambito di indagine, però, è a tutt’oggi vasto e spesso l’interpretazione dei risultati è complessa in quanto non tutte le alterazioni genetiche sono responsabili di patologie e la raccolta dei dati internazionali in merito non è ancora esaustiva. La tecnologia NGS ha permesso un salto qualitativo perché ha ridotto drasticamente i tempi di indagine: prima occorrevano uno o due anni per studiare due o tre grossi geni, con questa tecnologia c’è la possibilità di lavorare su una pluralità di geni contemporaneamente con tempi e costi ridotti».
Attualmente, le indagini genetiche non sono in grado di evidenziare la causa di tutte le malformazioni congenite o del ritardo mentale. « Il 50% delle patologie genetiche non ha ancora una causa definita. I tests citati precedentemente aumentano del 20% o più, la possibilità di diagnosticarne la causa. L’ambito di indagine, però, è a tutt’oggi vasto e spesso l’interpretazione dei risultati è complessa in quanto non tutte le alterazioni genetiche sono responsabili di patologie e la raccolta dei dati internazionali in merito non è ancora esaustiva. La tecnologia NGS ha permesso un salto qualitativo perché ha ridotto drasticamente i tempi di indagine: prima occorrevano uno o due anni per studiare due o tre grossi geni, con questa tecnologia c’è la possibilità di lavorare su una pluralità di geni contemporaneamente con tempi e costi ridotti».
Fino ad oggi sono state identificate più di 8000 malattie genetiche. Individuarne la causa permette di calibrare meglio la assistenza clinica e soprattutto di definire il rischio di ripetizione delle stesse patologie, nelle famiglie.
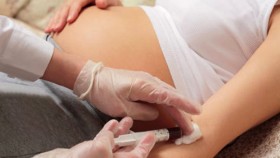
Una altra importante innovazione della ricerca genetica si registra nel campo ostetrico. Alcune indagini prenatali possono, infatti, essere effettuate in modo non invasivo con un semplice prelievo di sangue alla madre: « Attualmente, la diagnosi prenatale non invasiva (NIPD) è un’opportunità reale ma che non viene ancora riconosciuta dal Servizio Sanitario Nazionale, pertanto può essere effettuata soltanto privatamente e il costo è ancora elevato: tra gli 800 e i 2000 euro. Il test si basa sul sequenziamento del DNA fetale che circola libero nel sangue materno. È importante chiarire che è un test di screening e non diagnostico, per cui deve comunque essere integrato con gli altri test come la misurazione della translucenza nucale fetale, le ecografie morfologiche e le eventuali diagnostiche invasive, ad oggi ancora insostituibili nella gestione della gravidanza a rischio».
Il test NIPD si effettua attraverso un prelievo di sangue alla madre a partire dalla decima settimana di gravidanza. Con esso si individuano le trisomie dei cromosomi 21(Sindrome di Down) , 18 o 13, oppure le anomalie numeriche dei cromosomi sessuali (X o Y), ma non le alterazioni in singoli geni o altri tipi di anomalie cromosomiche non di numero ma di struttura che comportano perdite o duplicazioni di materiale genetico. La capacità di individuare le anomalie citate si aggira attorno al 99% ma c’è una percentuale di falsi positivi ( anche se meno dell’1%) e anche di falsi negativi ( sembra meno dello 0,2%). In caso di positività, dunque, si deve confermare il risultato mediante la villocentesi o la amniocentesi.
E’ molto importante che tutti i test genetici citati, e anche questo, siano accompagnati da una consulenza genetica pre test e a una post test per la interpretazione corretta dei risultati e dei limiti di essi. E’ possibile effettuare una “prima visita di genetica medica” all’ambulatorio di genetica medica dell’ Ospedale di Circolo con l’impegnativa del proprio medico curante. Attualmente in Italia, non si effettua il test che viene offerto da centri esperti prevalentemente negli Stati Uniti. Tra poco sarà tuttavia possibile appoggiarsi anche a due laboratori italiani, a Roma e a Pavia : « Entro uno o due anni – conclude il dottor Casalone – sarà possibile ampliare il campo di indagine includendo nelle possibilità diagnostiche anche altre anomalie cromosomiche o i cosidetti micro-riarrangiamenti citogenetici responsabili di sindromi quali la sindrome di Williams o di Di George».


